Биогенные элементы.
К числу биогенных относят те химические элементы, которые являются главными в составе тканей живых организмов. В первую очередь это углерод, водород, азот и фосфор, а если речь идет о водных экосистемах - еще и кремний, из которого строятся панцири диатомовых водорослей. Углерод поступает в водные экосистемы в виде углекислоты из атмосферы и превращается в органическую материю путем фотосинтеза, который осуществляется водорослями; этот элемент, наряду с водородом, не является дефицитным. Азот в усваиваемой организмами форме нитрат-иона и ионов аммония поступает в озера в основном из их водосборных бассейнов и из атмосферы, а частично - за счет деятельности некоторых сине-зеленых водорослей, способных утилизировать элементарный азот из атмосферы. Растворимые, усваиваемые организмами соединения фосфора поступают в озера с водами их притоков и с атмосферными осадками. Наконец, растворимые формы кремния поступают из водосборных бассейнов в результате выветривания горных пород. Кроме того, упомянутые биогенные элементы поступают в воду озер при разложении отмерших организмов из озерных осадков. Концентрации биогенных элементов в воде и их соотношения определяют трофический статус озер и качество вод. Многие озера вследствие вызванного деятельностью человека накопления избытка биогенных элементов (например, вследствие смыва удобрений) за очень короткие промежутки времени стали эвтрофными, то есть, избыточно богатыми живой материей. На поверхности эвтрофных озер происходит массовое цветение сине-зеленых водорослей, которые издают неприятный запах и иногда выделяют в воду токсины. Отмершая биомасса оседает на дно. Для ее разложения микроорганизмы используют кислород, забирая его из воды. При значительном падении концентрации растворенного кислорода происходит гибель придонных организмов, например, «замор» - массовая гибель - рыб. Среди биогенных элементов особая роль в эвтрофикации озер принадлежит фосфору (Vollenweider, 1968).
На рис. 2.4.1 показана динамика изменения концентрации фосфора в водах озера Бодензее. Можно видеть, что в конце 70-х годов эта концентрация достигла 80-90 микрограммов на литр. Это создало угрозу эвтрофикации Бодензее - одного из важнейших для Германии источников (130 млн. м3 в год) питьевой воды. Лимнологи обратили внимание на резкий рост концентрации фосфора в Бодензее и угрозу его эвтрофикации еще в 1959 году. Благодаря принятым законодательным мерам и изменению хозяйственной практики, с 1975 г. стало происходить снижение поступлений растворимого фосфора из городских очистных сооружений и из сельскохозяйственных рассеянных источников, и озеро стало возвращаться к исходному олиготрофному состоянию. Отметим, что объем Бодензее равен 50 км3, а сдвиг в сторону эвтрофикации произошел тогда, когда сброс растворимого фосфора превысил 500 тонн в год (рис. 2.4.1).
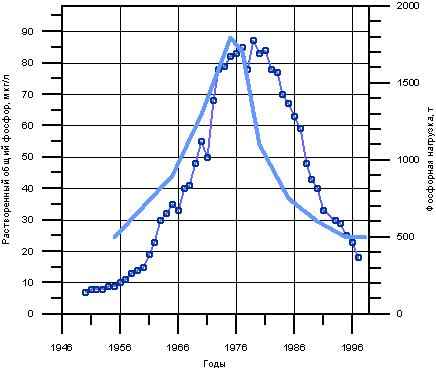
Рис. 2.4.1. Динамика изменения концентрации общего роастворенного фосфора в озере Бодензее. Измерения проводились в конце периодов интенсивного перемешивания. Серая сплошная линия - фосфорная нагрузка. Wagner 1996, 1997.
![]() Загрузить исходные данные в формате Grapher 3
Загрузить исходные данные в формате Grapher 3
В настоящем разделе дается оценка состояния Байкала с точки зрения возможности его эвтрофикации. Для того, чтобы дать такую оценку, необходимо прежде всего располагать долговременными рядами данных о концентрациях биогенных элементов. Измерения концентраций биогенных элементов и получение надежных усредненных данных затрудняются тем, что эти концентрации сильно изменяются во времени и пространстве.
На рис. 2.4.2 показана динамика изменения концентраций растворенного фосфора, нитратного азота и растворенного кремнезема в поверхностных водах Байкала в период с 1948 по 1955 г. (Вотинцев, 1961). Можно видеть, что концентрации сильно различаются в разные сезоны и годы. Снижение концентраций определяется расходом биогенных элементов на построение клеток планктонных водорослей, которые размножаются в верхнем 50-метровом слое благодаря проникающему на эту глубину солнечному свету, а затем под действием силы тяжести погружаются на дно, либо потребляются зоопланктоном. Рост концентраций биогенных элементов происходит тогда, когда глубинные воды в результате процессов вертикального перемешивания попадают на поверхность. Интересно отметить, что особенно резкое снижение концентраций всех биогенных элементов происходило в «мелозирные» годы (1950 и 1953), то есть в те годы, когда биомасса фитопланктона была максимальной (рис. 2.4.2). Однако полученные данные не поддаются количественной интерпретации, так как концентрации биогенных элементов зачастую снижались в те сезоны и годы, когда найденная биомасса фитопланктона была небольшой. Одним из таких сезонов, например, была осень 1948 года. Возможные причины такого несоответствия будут рассмотрены в разделе о планктоне. Приводим средние значения (по Вотинцеву, 1961) концентраций в слое 0-50 м и (после знака ±) величины стандартных отклонений: растворимый фосфор 21 ± 11 мкг/л; нитратный азот 45 ± 19 мкг/л; растворимый кремнезем 2,16 ±0,71 мг/л.
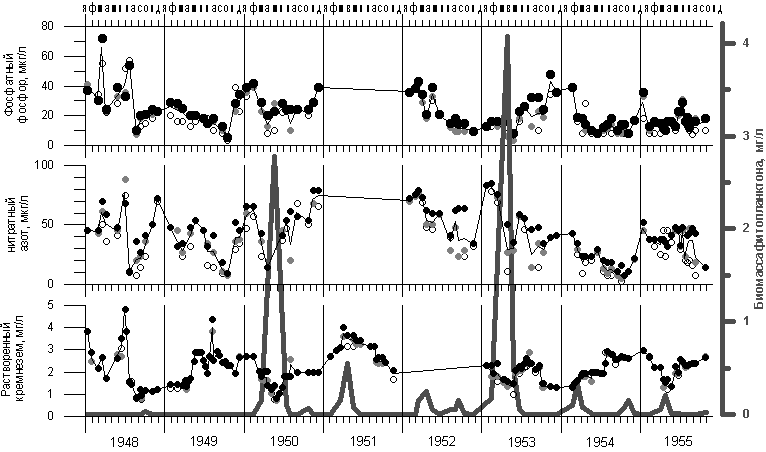
Рис. 2.4.2. Динамика изменения концентраций биогенных элементов в поверхностных водах Байкала. Светлые значки - 0 м, серые - 25 м, черные - 50 м, тонкие линии - средние для горизонтов 0 - 50 м, Вотинцев 1961. Толстая серая линия и правая ось ординат - биомасса фитопланктона (без пикопланктона), Kozhov 1963, p. 235. Методика химических измерений - см. Верещагин 1933.
![]() Загрузить исходные данные в формате Grapher 3
Загрузить исходные данные в формате Grapher 3
Биогенные элементы распределены в Байкале неравномерно по глубине. Это касается не только верхнего 50-метрового слоя, где биогенные элементы потребляются водорослями, но и глубинных вод. На рис. 2.4.3 и 2.4.4 показаны вертикальные профили распределения биогенных элементов, причем обычно имеет место повышение концентраций с глубиной. Такой градиент объясняется тем, что глубинные воды Байкала обновляются медленно (Weiss et al., 1991), за характерное время порядка 10 лет, а среднегодовые концентрации в верхнем слое постоянно понижены вследствие потребления водорослями. Глубинные воды поступают наверх тогда, когда поверхностные воды проникают в глубинные слои. Однако обновление глубинных вод происходит эпизодически. Видимо, следствием крупномасштабного проникновения поверхностных вод в глубинные слои была пониженная концентрация растворимого кремнезема на глубинах 1300-1400 м в Южном Байкале в июне 1991 года (рис. 2.4.4). Поверхностные воды в период, предшествовавший этому эпизоду, должны были быть сильно обеднены растворимым кремнеземом, так как 1990 год был «мелозирным».
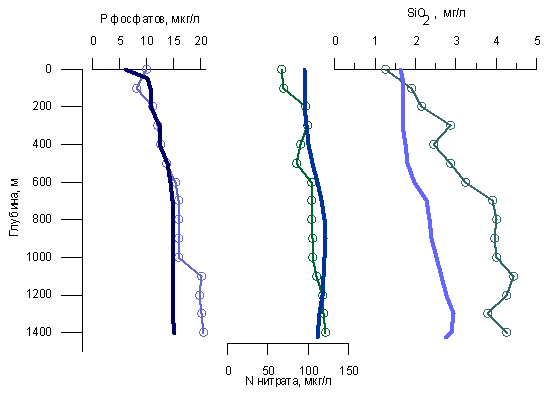
Рис. 2.4.3. Распределение биогенных элементов в Южном Байкале по глубинам (кривые с круглыми значками), данные Г.Ю. Верещагина, 1949г., середина лета. Цитируется по книге Kozhov 1963, p. 49. Толстые серые кривые - данные о концентрациях фосфатного фосфора, нитратного азота (Weiss et al., 1991) и растворимого кремнезема (Killworth et al., 1996) в Южном Байкале в июне 1988 г.
![]() Загрузить исходные данные в формате Grapher 3
Загрузить исходные данные в формате Grapher 3
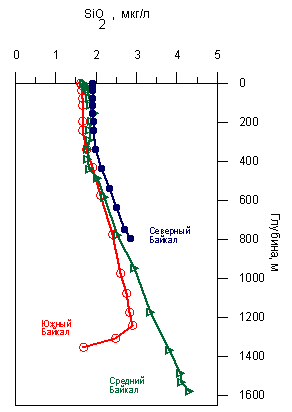
Рис. 2.4.4. Распределение растворимого кремнезема в Байкале в июне 1991 г. Falkner 1997. 1991 год был не-мелозирным, 1990 - мелозирным.
![]() Загрузить исходные данные в формате Grapher 3
Загрузить исходные данные в формате Grapher 3
Интересно сопоставить данные измерения концентраций биогенных элементов 1940-х гг., полученные колориметрическим методом с визуальной разностной оценкой, с данными, полученными в 1988-91 гг. с использованием современных спектрофотометров. В случае нитрата и фосфата данные различаются ненамного. Данные Г.Ю. Верещагина для глубин 1100-1400 м (рис. 2.4.3), вероятно, являются ошибочными, так как в противном случае нужно было бы предполагать, что концентрация фосфора в Южном Байкале за последние 50 лет заметно понизилась, для чего нет никаких причин. В свете современных данных следует считать ошибочными абсолютные результаты режимных наблюдений 1948-1955 гг. (рис. 2.4.2), так как найденная средняя концентрация фосфата в верхнем слое, равная 21 мкг/л, существенно выше максимальной концентрации фосфата в Южном Байкале, определенной современным методом, а максимальные пиковые концентрации, как видно из того же рисунка, достигали значений 40-60 мкг/л, хотя они не могут быть выше тех, которые имеются в глубинных водах. По-видимому, методика измерения концентраций «фосфатов» 1948-55 гг. содержала источник систематической ошибки. К сожалению, попыток прямого сопоставления результатов, получаемых новым и старым методами, насколько известно автору настоящего обзора, не предпринималось.
Из данных, приведенных на рис. 2.4.2, можно заключить, что систематическая ошибка присутствовала в ранних работах и при измерении концентраций растворимого кремнезема. По-видимому, с тем же источником систематической ошибки имел дело К.К. Вотинцев, в обзоре которого, опубликованном в 1992 г. (Вотинцев, 1992а), указано, что концентрация кремния в верхних слоях воды составляет 0,8-1,3 мг/л, а на максимальных глубинах достигает 1,7-2,5 мг/л, что соответствует диапазону от 1,7 до 5,4 мг/л растворимого SiO2. Метод Мортлока, примененный (Killworth et al., 1996), гарантирует точность и правильность измерения растворимого кремнезема в пределах 0,01 мг/л (Falkner et al.,1997). Поэтому данные, представленные на рис. 2.4.3, согласно которым градиент концентрации растворенного SiO2 в водах Южного Байкала имеет диапазон от 1,5 до 2,5 мг/л, представляются вполне достоверным.
Из сказанного выше ясно, что из-за природной изменчивости концентраций биогенных элементов и систематических расхождений между данными старых и новых методов для Байкала не могут быть построены графики, подобные показанным на рис. 2.4.1, для Боденского озера.
На рис. 2.4.5 приведена схема годового баланса озера Байкал по фосфору, подсчитанного (Callender, Granina, 1997) в основном по опубликованным ранее данным российских исследователей. В этой же статье дан подробный обзор соответствующей литературы. Можно видеть, что общее количество фосфора в водном теле Байкала составляет 398 килотонн. В биологической продукции ежегодно участвует 80 килотонн этого элемента. Из этого количества 75 килотонн реминерализуется в водной толще, в осадках захоранивается 3,4 килотонны. Из осадков в водную толщу поступает 2,2 килотонны фосфора за счет процессов гидролиза и последующей диффузии, то есть в растворенном состоянии.
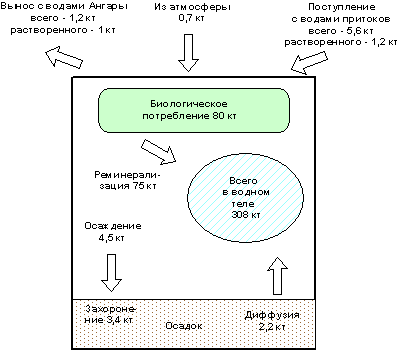
Рис. 2.4.5. Баланс фосфора в Байкале. Callender, Granina 1997.
В озеро с водами притоков ежегодно поступает 1,2 килотонны растворенного фосфора, а воды Ангары выносят из него 1 килотонну растворенного фосфора. Из атмосферы в растворенном состоянии поступает 0,7 килотонны. Таким образом, всего в Байкал ежегодно поступает 4,1 килотонны растворенного фосфора. Эта величина всего в 8 раз больше той фосфорной нагрузки (0,5 килотонны), которая считается приемлемой для поддержания олиготрофного состояния озера Бодензее, хотя объем этого озера в 460 раз меньше объема Байкала. В водном теле Бодензее находится всего около 1,3 килотонны растворенного фосфора, что в 2,6 раз больше годовой фосфорной нагрузки на это озеро. Запас растворенного фосфора в Байкале больше годовой нагрузки в 80 раз. Очевидно, что непосредственной угрозы эвтрофикации Байкала пока нет. К точно такому же выводу на основании несколько иных соображений в 1992 г. пришел К.К.Вотинцев (Вотинцев, 1992).
Следует с осторожностью рассматривать высказываемые некоторыми специалистами соображения о признаках изменения трофического статуса Байкала. Например, в работе (Callender, Granina, 1997) цитируют данные Тарасовой и Мещеряковой (1992), согласно которым к концу 80-х гг. в Байкале исчез характерный для 60-х гг. градиент «органического фосфора» от 8 мкг/л в поверхностных до 3 мкг/л в глубинных водах, и его концентрация на всех глубинах стала равной 8 мкг/л. Источник необходимых для этого 80 килотонн фосфора, неизвестен.
Измерения концентраций фосфора в практике организаций, публикующих данные нем в Байкале и его притоках, метрологически плохо обеспечены. Это касается как измерений собственно ортофосфат-аниона, так и в особенности «органического» и «общего» фосфора, так как не стандартизована процедура фильтрации проб, предшествующая анализам. Правильность балансовых оценок о поступлении в Байкал элементов со взвешенными веществами трудно оценить, так как их авторы (например, Callender, Granina, 1997a) не дают строгого определения границ Байкала. Точные балансовые оценки могут быть получены лишь при регулярных одновременных режимных наблюдениях за стоком рек (а в дельте Селенги - и ее проток) в местах их впадения в Байкал и концентрациями веществ с помощью метрологически обеспеченных методик. Такие наблюдения на Байкале пока не ведутся.
По-видимому, представления (Vollenweider, 1968) об особой роли фосфора в эвтрофикации озер, приведшие к массовому строительству установок для удаления фосфора на очистных сооружениях, верны не всегда. Например, Брукс и Эджингтон (Brooks, Edgington, 1994) выдвинули интересные соображения в пользу того, что в озере Мичиган в отношении растворенного фосфора поддерживается естественный гомеостаз, то есть его концентрация в водном теле и тем самым трофический уровень озера не зависят от тех количеств фосфора, которые поступают от многочисленных муниципальных очистных сооружений. Они обратили внимание на то, что концентрация "растворенного реакционноспособного фосфора" (ортофосфат-аниона) в озере Мичиган остается в течение года постоянной на уровне около 0,02 мкМ, хотя концентрация общего растворенного фосфора, растворенного кремнезема, хлорофилла вследствие деятельности фитопланктона регулярно меняется от зимы к лету в несколько раз (рис. 2.4.6). Они подсчитали, что все источники поступления фосфора вместе дают не более 2 ммоль Р на квадратный метр в год, в то время как для обеспечения наблюдаемого весеннего роста общего фосфора необходимо не менее 27 ммоль этого элемента на квадратный метр. Отсюда ясно, что источником фосфора, поступающего весной в озеро, должно было быть его дно. Зная рН вод озера Мичиган (8,2), концентрацию ионов кальция (870 мкМ) и концентрацию ортофосфата (0,02 мкМ), они подсчитали, что эта вода является насыщенным раствором ок-сиапатита Са10(PO43-)6(ОН-)2: оказалось, что произведение ассоциации ионов для вод Мичигана имеет вид
Логарифм произведения растворимости для чистого оксиапа-тита равен -114, а для оксиапатита в природных средах варьирует в пределах от -122 до -100. Опираясь на эти данные, Брукс и Эджингтон считают, что определенное количество оксиапатита всегда находится в осадках озера Мичиган. Ветровое перемешивание приводит к тому, что ортофосфат постоянно поддерживается в равновесной концентрации относительно оксиапатита. Удаление ортофосфата из раствора фитопланктоном вызывает смещение равновесия, и часть оксиапатита растворяется. Экскреция фосфата потребителями фитопланктона и организмами высших звеньев пищевой цепи, а также его поступление из водосборного бассейна и с очистных сооружений приводят к накоплению оксиапатита в осадках. Благодаря этому механизму экосистема озера Мичиган защищена от резких колебаний при изменении внешней фосфорной нагрузки (рис. 2.4.6).
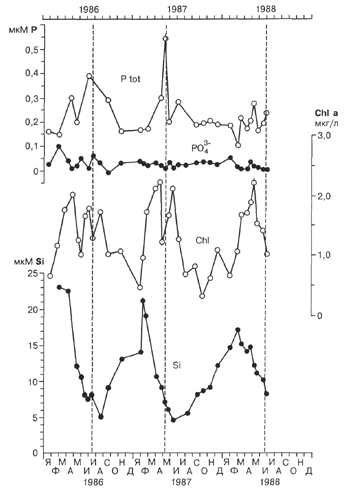
Рис. 2.4.6. Динамика изменения концентраций оющего растворенного фосфора (P tot), ортофосфата, хлорофилла a и растворенного кремния в водах озера Мичиган (по данным Brooks, Edgington, 1994).
С другой стороны, на внутреннюю фосфорную нагрузку и состояние (трофность) экосистемы могут влиять метеоусловия, и в том числе колебания уровня озера, изменяющие интенсивность взмучивания донных осадков. Не исключено, что относительно озера Байкал можно говорить о гомеостазе, поддерживающем постоянную концентрацию ортофосфата в глубинных водах. Концентрация ортофосфата в глубинных водах Байкала равна 0,5 мкМ (Weiss et al., 1991), а ионов кальция - 400 мкМ (Falkner et al., 1991), рН варьирует в пределах 7,5-8. Расчет показывает, что в этих условиях ортофосфат также может находиться в равновесии с оксиапатитом (lg KiAP = -108). Различие, однако, состоит в том, что Байкал не перемешивается ветром до дна, и поэтому в верхнем слое наблюдается значительно меньшая концентрация ортофосфата (0,15-0,2 мкМ). Рассмотренный механизм, если он верен, делает устойчивость озера Байкал к внешней фосфорной нагрузке еще более высокой. В заключение заметим, что об удовлетворительном трофическом статусе Байкала свидетельствует то, что его воды на всех глубинах, в том числе и придонные, на всех изученных станциях содержат кислород в высоких концентрациях - от 9,6 до 12,8 мг/л, или от 87 до 11О % от насыщающей (см., например, Killworth et al., 1996). Более того, благодаря многолетним исследованиям Л.З. Граниной, определившей глубину залегания окисленного слоя осадков с повышенными концентрациями железа и марганца по всей площади дна Байкала, хорошо известно (Атлас Байкала, 1993), что кислород повсеместно проникает на небольшую глубину и в донные отложения. Этот факт был недавно подтвержден исследованиями, выполненными с помощью микроэлектродов (Martinet al., 1993; 1998).
Перепечатка без согласия автора запрещена. E-mail для контактов: grachev@lin.irk.ru
Публикация книги в сети интернет выполнена по гранту РФФИ-байкал №05-07-97200 E-mail: jonin@lin.irk.ru



